
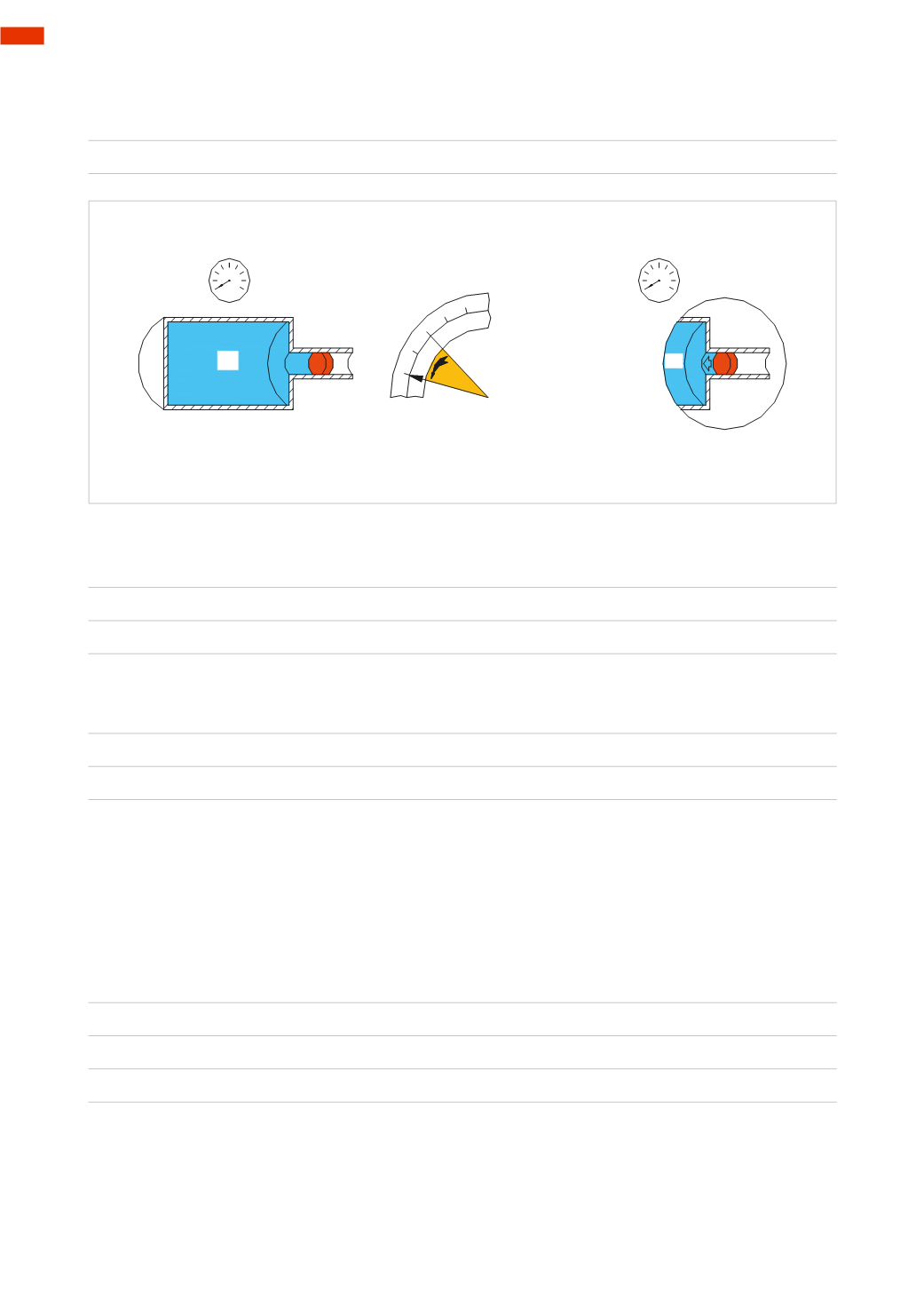
Figura 13
Riducendo la temperatura, all’interno del serbatoio si ha una contrazione delle molecole, si crea una specie di
vuoto, il pistone è attirato verso l’interno finché non si ristabilisce l’equilibrio della pressione.
P
1
:
P
2
=
T
1
:
T
2
0
20
40
273 K
V
1
V
2
Fig. 13
Esempio 1
: un gas occupa un volume di 0,5
m
3
alla temperatura di 283
K
, quale sarà il suo volume a 323
K
se
rimane costante la pressione?
V
1
= 0,5
m
3
T
1
= 283
K
T
2
= 323
K
V
2
= ?
V
1
:
V
2
=
T
2
:
T
1
0,5
:
V
2
= 283 : 323
V
2
= (0,5 * 323) / 283 =
0,57
m
3
Esempio 2
: una bombola è piena di gas ad una pressione di 2
bar
ed a una temperatura di 283
K
, rimanendo
esposta al sole si riscalda di 50
°C
. Che pressione si avrà all’interno della bombola?
P
1
= 2
bar
T
1
= 283
K
P
2
= ?
T
2
=
T
1
+ 50 = 333
K
P
1
:
P
2
=
T
1
:
T
2
2
:
P
2
= 283 : 333
P
2
= (2 * 333) / 283 =
2,35
bar
Relazione tra pressione, volume e temperatura
Come dimostrato in precedenza tra Pressione, Volume e Temperatura esiste un legame indissolubile: al modificarsi
dell’una si modificano anche le altre. Riassumiamo le loro relazioni:
V
1
:
V
2
=
p
2
:
p
1
(legge di Boyle) a temperatura costante
V
e
p
sono inversamente proporzionali
V
1
:
V
2
=
t
1
:
t
2
(1
a
di Gay-Lussac) a pressione costante
V
e
t
sono direttamente proporzionali
p
1
:
p
2
=
t
1
:
t
2
(2
a
di Gay-Lussac) a temperatura costante
p
e
t
sono direttamente proporzionali
Utilizzando queste relazioni si risolve il seguente problema:
un cilindro con diametro interno
d
= 50
mm
è riempito con un gas che alla temperatura
t
1
= 20
°C
occupa un
volume
V
1
= 0,98
dm
3
; sullo stelo è applicato un carico
F
1
= 980
N
. Calcolare lo spostamento del pistone al
raddoppio del carico (
F
2
= 2 *
F
1
) ed a una temperatura ambiente
t
2
= 50
°C
.
Calcolo del volume raggiunto dal gas.
1
22
CAMOZZI
>
LA FISICA

















